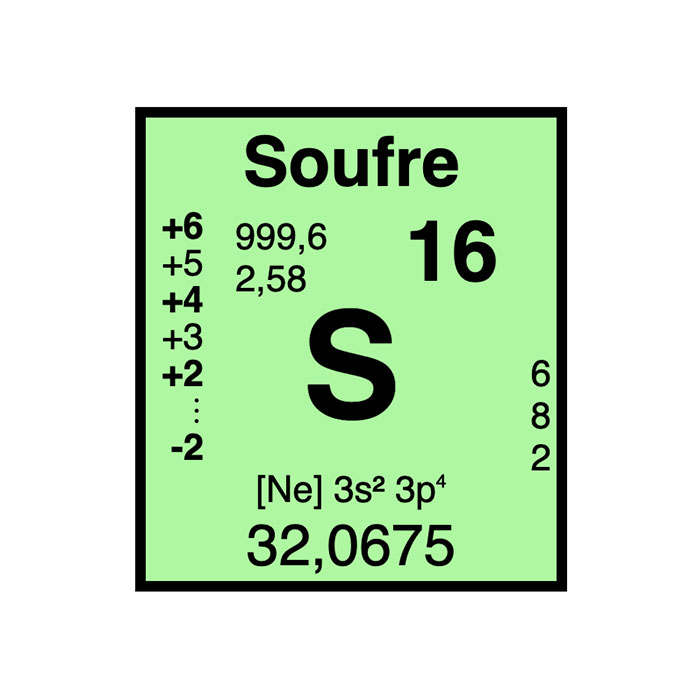
Caractéristiques du soufre
- Symbole : S
- Masse atomique : 32,065 ± 0,005 u
- Numéro CAS : 7704-34-9
- Configuration électronique : [Ne]3s23p4
- Numéro atomique : 16
- Groupe : 16
- Bloc : Bloc P
- Famille d’éléments : Non-Métal
- Électronégativité : 2,58
- Point de fusion : 115,21 °C


