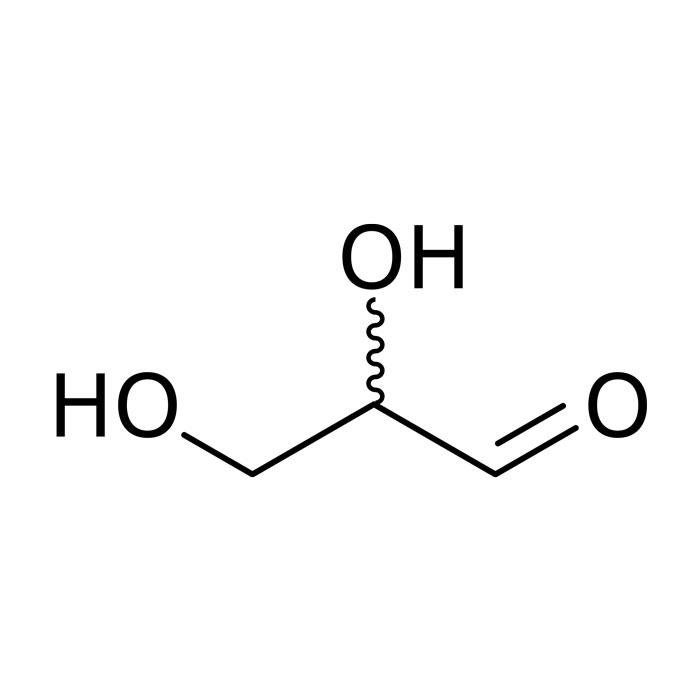
Caractéristiques du Triose
-
Identification du triose :
- Nom UICPA : –
- Synonymes : –
- N° CAS : –
- N° ECHA : –
- N° CE : –
- Code ATC : –
- PubChem : –
- ChEBI : –
- FEMA : –
- SMILES :–
- InChl : –
Propriétés chimiques :
- Formule : C3H6O3
- Masse molaire : –
- pKa : –
Propriétés physiques :
- T° Fusion : –
- Solubilité : –
Propriétés biochimiques :
- Codons : –
- pH isoélectrique : –
- Acide aminé essentiel : –
- Occurrence chez les vertébrés : –
Propriétés optiques :
- Pouvoir rotatoire : –
Précautions :
- SIMDUT : –
