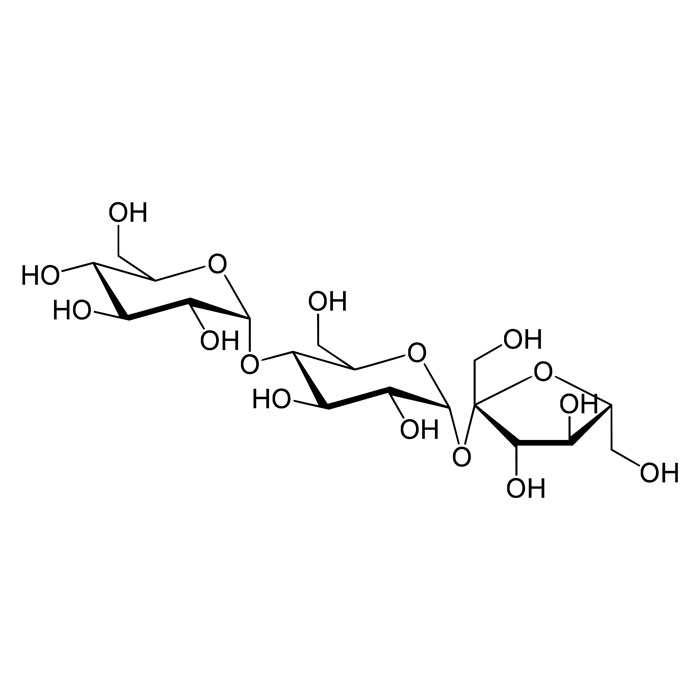
Caractéristiques de l’erlose
-
Identification de l’erlose :
- Nom UICPA : (2R,3R,4S,5S,6R)-2-[(2R,3S,4R,5R,6R)-6-[ (2S,3S,4S,5R)-3,4-dihydroxy-2,5-bis(hydroxymethyl)oxolan- 2-yl]oxy-4,5-dihydroxy-2-(hydroxymethyl)oxan-3- yl]oxy-6-(hydroxymethyl)oxane-3,4,5-triol
- Synonymes : Glucosylsucrose, sucrosylglucose, alpha-Maltosyl bêta-fructofuranoside, 4 G -alpha-D-glucopyranosyl sucrose
- N° CAS : 13101-54-7
- N° ECHA : –
- N° CE : 878-478-2
- Code ATC : –
- PubChem : 193471
- ChEBI : 55512
- FEMA : –
- SMILES :C(C1C(C(C(C(O1)OC2C(OC(C(C2O)O)OC3(C( C(C(O3)CO)O)O)CO)CO)O)O)O)O
- InChl : 1S/C18H32O16/c19-1-5-8(23)10(25)12(27)16(30 -5)32-14-7(3-21)31-17(13(28)11(14)26)34-18(4-22) 15(29)9(24)6(2-20)33-18/h5-17,19-29H,1-4H2 /t5-,6-,7-,8-,9-,10+,11-,12-,13-,14-,15+, 16-,17-,18+/m1/s1
Propriétés chimiques :
- Formule : C18H32O16
- Masse molaire : 504,437 1 ± 0,021 4 g/mol
- pKa : 12.70±0.70
Propriétés physiques :
- T° Fusion : 80,0 à 80,5 °C (forme hydratée I) et 136,5 à 137,0 °C (forme hydratée II)
- Solubilité : 1 400–1 500 g·L-1 à 25 °C
Propriétés biochimiques :
- Codons : –
- pH isoélectrique : –
- Acide aminé essentiel : –
- Occurrence chez les vertébrés : –
Propriétés optiques :
- Pouvoir rotatoire : –
Précautions :
- SIMDUT : –




















