L’alanine ou L-alanine est un acide aminé non essentiel que le corps peut synthétiser par lui-même. Elle est naturellement présente dans divers aliments, tant d’origine animale que végétale. Bien que l’organisme puisse en produire, des apports supplémentaires peuvent être bénéfiques, surtout pour les personnes pratiquant une activité sportive intense.
Description de l’alanine
L’alanine, également appelée acide amino-2-propanoïque, est impliquée dans la construction des protéines. Avec la proline, elle constitue l’un des deux seuls acides aminés que le corps est en mesure de produire par lui-même en quantité suffisante, sans avoir besoin d’apport extérieur. Elle est synthétisée à partir d’autres acides aminés comme la leucine, la valine et l’isoleucine.
La L-alanine joue un rôle essentiel dans le bon fonctionnement de l’organisme en contribuant à plusieurs aspects vitaux. Cet acide aminé participe notamment à la décomposition du tryptophane et de la vitamine B6. De plus, il est crucial pour la formation des globules blancs, éléments clés du système immunitaire.
Par ailleurs, cet aminoacide favorise une meilleure utilisation du glucose par le corps, aidant ainsi à prévenir l’hypoglycémie. Des études suggèrent même que l’acide amino-2-propanoïque pourrait être bénéfique dans le traitement de certains types de diabète.
Historique de l’alanine
La découverte de l’alanine remonte à 1850, grâce à Adolph Strecker, un chimiste allemand. Ce dernier tentait à l’origine de créer de l’acide lactique à travers une réaction chimique impliquant de l’acétaldéhyde, de l’ammoniac et du cyanure d’hydrogène. Depuis, ce processus est connu sous le nom de « synthèse de Strecker ».
Par la suite, en 1875, Paul Schützenberger, un chimiste français, a réalisé une expérience de décomposition de la soie en utilisant de la baryte dans un autoclave. Cela lui a permis d’identifier un mélange d’acides aminés comprenant de la glycine et de l’alanine. Dans la composition des chaînes protéiques analysées, cette dernière est présente à hauteur d’environ 29,7 %.
Ces découvertes ont grandement contribué à la compréhension de la synthèse et du rôle des acides aminés dans la formation des protéines qui composent le corps humain.
Structure de l’alanine
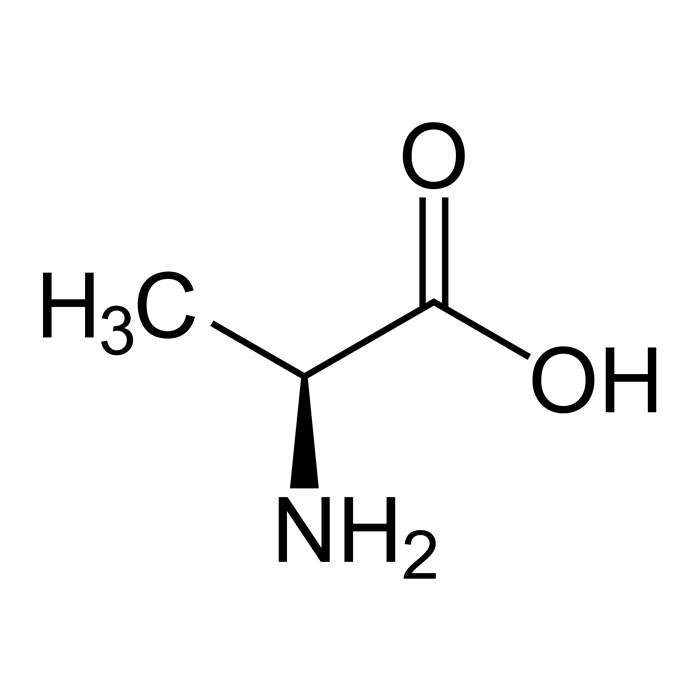
À l’instar de tous les autres aminoacides, l’alanine présente deux groupes fonctionnels : un groupe carboxyle (COOH) et un groupe amine (NH2). Sa particularité réside dans sa chaîne latérale, la plus simple après celle de la glycine, puisqu’elle est constituée uniquement d’un groupement méthyle (-CH3).
En raison de ses propriétés, la L-alanine est classée comme un acide aminé hydrophobe aliphatique. Autrement dit, elle a une affinité pour les environnements non polaires tels que les zones insolubles dans l’eau.